
Il sunitinib è un farmaco antitumorale usato per il trattamento del carcinoma renale (CCR) metastatico e in tumori gastrointestinali stromali (GIST) resistenti o intolleranti a imatinib.
MECCANISMO DAZIONE
Sunitinib è un inibitore multi-target degli enzimi tirosina-chinasi, autorizzato in Italia come seconda linea di trattamento per il tumore stromale gastrointestinale (GIST) e come prima e seconda linea per il carcinoma renale avanzato e/o metastatico (MRCC).
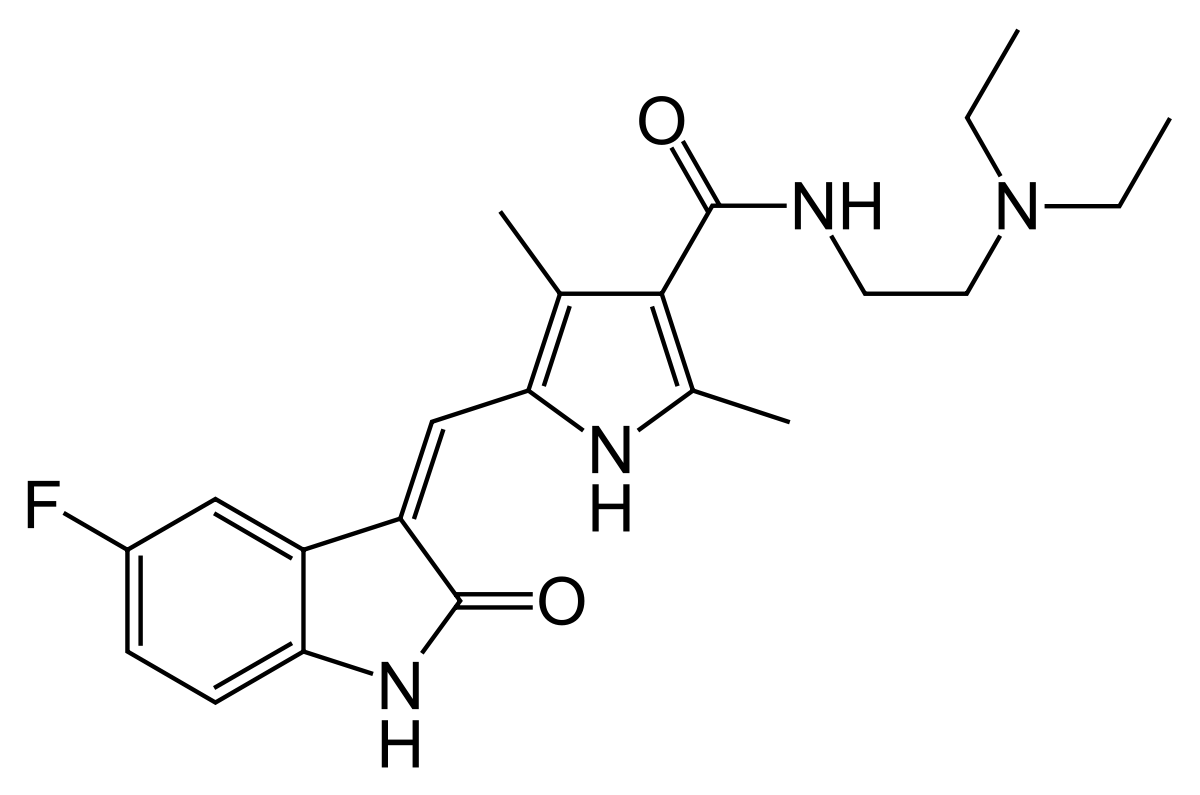
Sunitinib (Sutent) è un farmaco a basso peso molecolare, capace di inibire selettivamente alcune proteine essenziali per la crescita e proliferazione di cellule a fenotipo mutato.
Queste strutture molecolari sono le cosiddette Tirosin Kinasi (TK), ovvero enzimi che inviano segnali di crescita e di divisione alle cellule.
|
|
Nellambito dello studio genetico delle cause di proliferazione maligna incontrollata, i biologi ricercatori hanno scoperto una mutazione del gene che porta allespressione delle Tirosin Kinasi. Ciò comporta la sintesi da parte della cellula neoplastica di enzimi che presentano unattività molto più elevata del normale, cui ne consegue la formazione della massa tumorale maligna.
Inoltre, in queste cellule mutate, viene inibita lattivazione dei meccanismi difensivi di morte cellulare programmata.
Il sunitinib è un inibitore competitivo delle tirosinokinasi, che interagendo con esse, impedisce che i segnali biochimici che lorganismo invia vengano tradotti in una risposta proliferativa, impedendo lo sviluppo del tumore (inibendo lazione del FLT3 fattore proliferativo) ed anche devascolarizzando la massa tumorale andando a bloccare la neoangiogenesi (inibizione di VEGF fattore pro neo vascolarizzante) impedendo che le cellule malate siano rifornite di nutrienti.
EFFETTI COLLATERALI SULLA TIROIDE
Il sunitinib può indurre ipotiroidismo sub-clinico e per questo è consigliato un accurato monitoraggio della funzione tiroidea durante il trattamento.
In considerazione di ciò, alcuni ricercatori belgi (Wolter, Stefan, Decallonne et al.) hanno condotto uno studio osservazionale prospettico per definire lincidenza e la severità di ipotiroidismo in pazienti con CCR o GIST in trattamento con sunitinib.
La funzione tiroidea è stata valutata prima e ai giorni 1 e 28 di ogni ciclo di trattamento.
Anticorpi anti-tiroidei sono stati determinati prima del trattamento e durante il follow-up, se si manifestava una funzione tiroidea anormale.
Sedici pazienti (27%) hanno sviluppato ipotiroidismo clinico o sub-clinico, che ha richiesto terapia sostitutiva, e 20 pazienti (34%) hanno manifestato aumento dei livelli di ormone stimolante la tiroide (TSH) che non ha richiesto intervento terapeutico.
Venti pazienti (34%) non hanno sviluppato anormalità tiroidee di tipo biochimico. |
|
Quindi, secondo questo studio belga, sunitinib può indurre ipotiroidismo sub-clinico, giustificando uno stretto monitoraggio della funzionalità tiroidea.
Anche ricercatori della Cleveland Clinic hanno analizzato la funzione tiroidea nei pazienti con carcinoma a cellule renali, metastatico, con lobiettivo di scoprire la causa del senso di fatica e astenia, associato al trattamento con lantitumorale Sunitinib.
I pazienti in trattamento presso il Cleveland Clinic Taussing Cancer Center erano in totale 73.
Lanalisi compiuta sui dati di 66 pazienti ha mostrato che l85% (n = 56) presentava una o più anomalie della funzione tiroidea.
L84% ( n = 47) dei pazienti con test di funzione tiroidea anomalo presentava segni e sintomi di ipotiroidismo.
Diciassette pazienti sono stati trattati con terapia di sostituzione tiroidea ed i sintomi sono migliorati in 9 soggetti.
Pertanto è ormai assodato che Sunitinib ed anche sorafenib, approvati per il trattamento del carcinoma renale metastatico e dellepatocarcinoma, sono associati a diversi gradi di alterazione della funzione tiroidea.
La prevalenza di ipotiroidismo indotto da sunitinib è differente nelle varie casistiche (50-85% negli studi retrospettivi; 36-46% in quelli prospettici), mentre lipotiroidismo è stato riportato in circa il 18% dei pazienti trattati con sorafenib.
È stato anche evidenziato che pazienti già ipotiroidei in trattamento sostitutivo con levotiroxina (L-T4), trattati con sunitinib e imatinib, e più recentemente anche con motesanib, possono richiedere un incremento della dose sostitutiva di L-T4.
Alla base di tale alterazione sembrerebbero esserci diversi meccanismi:
- ridotta sintesi di ormoni tiroidei, da correlare allinibizione della tireo-perossidasi e alla progressiva deplezione della riserva ormonale della ghiandola;
- inibizione della captazione di iodio;
- atrofia ghiandolare indotta dal TKI attraverso linibizione della vascolarizzazione o linduzione di una tiroidite (azione diretta sul VEGF);
- inibizione di VEGF-R e/o di altri possibili target (es. cKit, BRAF, RET).
È importante sottolineare come non sempre ci sia correlazione tra quadro ecografico, alterata funzione tiroidea da TKI e positività degli anticorpi anti-tiroide e che tali alterazioni possono passare attraverso fasi di iper- e ipotiroidismo.
Lipertiroidismo da sunitinib è però generalmente una condizione meno frequente dellipotiroidismo e che tende a regredire spontaneamente e pertanto non necessiterebbe di trattamento specifico.
La fatigue ovvero il senso di affaticamento e spossatezza del paziente neoplastico è un effetto collaterale di molteplici terapie anti-tumorali tra cui anche i TKI. Pertanto in presenza di tale sintomo la funzione tiroidea va sempre e comunque indagata.
È giusto comunque sottolineare che lipotiroidismo di per sé non richiede linterruzione della terapia con TKI e che la comparsa di ipotiroidismo sembrerebbe correlarsi a successo terapeutico.
Nei pazienti tiroidectomizzati in terapia con sorafenib, si possono osservare una diminuzione del rapporto T3/T4 e T3/rT3 e un aumento dei livelli di TSH.
Negli studi sui ratti, sunitinib sembrerebbe indurre una riduzione dei livelli ematici di T4 e T3, un aumento dellattività della desiodasi-3 (DIO3) e una diminuzione dellattività della desiodasi-1 (DIO1), associata ad una marcata riduzione della vascolarizzazione capillare della ghiandola.
È stato ipotizzato che nei pazienti tiroidectomizzati motesanib e vandetanib potrebbero essere in grado di aumentare il metabolismo della L-T4 attraverso un aumento di attività della DIO3 nei tessuti periferici, mentre l'ipotiroidismo è raro nei pazienti con tiroide in situ.
Inoltre,nei pazienti in trattamento con sunitinib, è possibile osservare non solo la diminuzione del rapporto T3/rT3 e un aumento dei livelli di TSH (circa il raddoppio), ma che dopo la sospensione del farmaco è possibile osservare la normalizzazione dellattività della DIO3 con associati bassi livelli di ormoni tiroidei.
È stato appurato anche che l'inibizione dell'angiogenesi potrebbe alterare il metabolismo periferico degli ormoni tiroidei.
Sempre negli studi sui ratti, l'espressione del gene DIO3 aumenta sotto lo stimolo ipossico-ischemico.
Se questa via di attivazione venisse provata anche nelluomo, la differenza nel tasso di ipotiroidismo osservabile con sunitinib rispetto a quello indotto da motesanib e vandetanib potrebbe essere ulteriormente giustificata dalla diversa affinità che i farmaci hanno nei confronti delle chinasi dei diversi recettori angiogenici.
Da questi studi si evince la necessità di un approccio multidisciplinare del paziente oncologico in trattamento con TKI, che richiede un attento follow-up della funzione tiroidea.
In particolare, si raccomanda unattenta sorveglianza della funzione tiroidea in tutti i pazienti prima di cominciare il trattamento specifico con TKI inibitori e ogni 2 cicli di trattamento, al fine di impostare sin dallinizio un adeguato protocollo di trattamento.
BIBLIOGRAFIA:
1. Makita N, Iiri T. Tyrosine kinase inhibitorinduced thyroid disorders: A review and hypothesis. Thyroid 2013, 23: 151-9. 11. Baldelli R, Barnabei A, Paoloni A, et al. Target therapy nei tumori tiroidei avanzati.
2. Lodish MB, Stratakis CA. Endocrine side effects of broad-acting kinase inhibitors. Endocr Relat Cancer 2010, 16: 233-44.
3. Desai J, Yassa L, Marqusee E, et al. Hypothyroidism after sunitinib treatment for patients with gastrointestinal stromal tumors. Ann Int Med 2006, 145: 6604.
4. Mannavola D, Coco P, 4.Vannucchi G, et al. A novel tyrosine-kinase selective inhibitor, sunitinib, induces transient hypothyroidism by blocking iodine uptake. J Clin Endocrinol Metab 2007, 92: 3531
5. Torino F, Corsello SM, Longo R, et al. Hypothyroidism related to tyrosine kinase inhibitors: an emerging toxic effect of targeted therapy. Nature Rev Clin Oncol 2009
6. Abdulrahman RM, Verloop H, Hoftijzer H, et al. Sorafenib-induced hypothyroidism is associated with increased type 3 deiodination. J Clin Endocrinol Metab 2010, 95: 375862.
7. Schlumberger MJ, Elisei R, Bastholt L, et al. Phase II study of safety and efficacy of motesanib in patients with progressive or symptomatic, advanced or metastatic medullary thyroid cancer. J Clin Oncol 2009, 27: 3794801.
8. The clinical implications of sunitinib-induced hypothyroidism: a prospective evaluation P Wolter1, C Stefan1, B Decallonne2, H Dumez1, M Bex2, P Carmeliet3,4 and P Schöffski11Department of General Medical Oncology, 2Department of Endocrinology, University Hospital Gasthuisberg, Catholic University Leuven, Leuven Cancer Institute, 3Center for Transgene Technology and Gene Therapy, K.U. Leuven, Leuven, 4Department for Transgene Technology and Gene Therapy, VIB Leuven, Leuven, Belgium British Journal of Cancer 2008; Volume 99, Number 3, August 5: Pages 448 454
9) AME FLASH n.18 di Luglio 2013
- TORNA SU -